突破性进展:基因疗法首次用于听力损失
2026年4月23日,美国食品药品监督管理局(FDA)批准了再生元制药(Regeneron)的基因疗法Otarmeni(开发代号DB-OTO),用于治疗OTOF基因突变导致的遗传性听力损失。这是首个获批治疗遗传性听力损失的基因药物,标志着听力医学的重大突破。
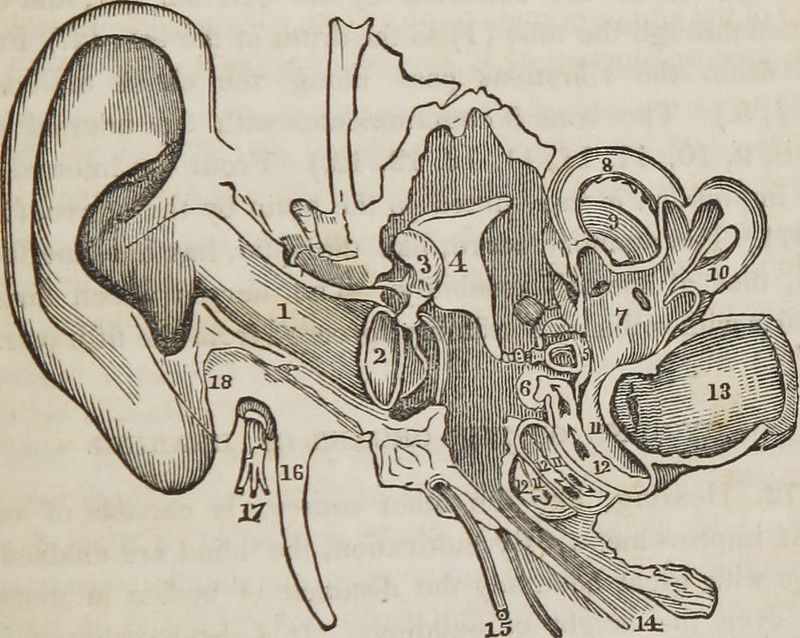
疾病背景:OTOF基因突变与听力损失
OTOF基因编码一种名为otoferlin的蛋白质,这种蛋白质在耳蜗内毛细胞中表达,负责调节内耳感觉细胞与听神经之间的信号传递。当OTOF基因发生突变时,患者无法产生功能性otoferlin蛋白,导致听力障碍。这种疾病极为罕见,美国每年约50名新生儿被诊断。
治疗原理:一次输注有望恢复自然听觉
Otarmeni利用工程改造的病毒作为载体,将正常拷贝的OTOF基因递送至耳蜗内毛细胞。患者在全身麻醉下接受耳蜗内输注,操作过程与人工耳蜗植入类似。输注后细胞利用该基因产生功能性otoferlin蛋白,从而恢复信号传导。该疗法为一次性治疗,旨在恢复自然的声学听力,避免传统人工耳蜗的“机器人音质”。
临床试验结果
关键临床试验(CHORD研究)纳入25名10个月至16岁的患者,排除治疗耳已植入人工耳蜗者。中期结果显示:
- 12名可评估患者中,11名听力出现有临床意义的改善,其中3名达到正常听力水平。
- 长期随访显示8名患者听力稳定或持续改善。
- FDA最终评价:20名可评估患者中80%听力得到改善。
定价与商业策略
再生元公司宣布将免费提供Otarmeni疗法,但此次批准附带一张“罕见儿科疾病优先审评券”,公司可将其出售给其他制药企业,预计价值数亿美元。